| Descripció |
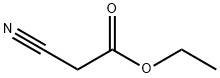
El cianoacetat d'etil és l'èster etílic de l'àcid cianoacètic. El cianoacetat d'etil s'hidrolitza ràpidament en condicions neutres i alcalines a àcid cianoacètic i etanol (i així ho fa en la majoria de condicions fisiològiques i ambientals), mentre que en pH àcid la vida mitjana és considerablement més llarga.
S'informa de la condensació de Knoevenagel de cianoacetat d'etil amb aldehid. S'informa de la reacció de condensació de Knoevenegal millorada al microones de cianoacetat d'etil amb un aldehid, P2O5, piperidina i clorobenceno. |
| Propietats químiques |
El cianoacetat d'etil és un líquid de color incolor a palla amb una suau olor agradable |
| Usos |
El cianoacetat d'etil es pot utilitzar en la síntesi de glioxilat d'etil. Es va utilitzar per investigar les reaccions de condensació de Knoevenagel al microreactor mitjançant catalitzadors de zeolita obtinguts empeltant grups amino a zeolites NaX i CsNaX. |
| Usos |
Reactiu utilitzat en la síntesi de pirimidina i purina marcada. El cianoacetat d'etil és un èster. Es pot utilitzar en la síntesi de glioxilat d'etil. Es va utilitzar per investigar les reaccions de condensació de Knoevenagel en microreactors utilitzant catalitzadors de zeolita obtinguts empeltant grups amino sobre zeolites NaX i CsNaX. |
| Preparació |
El cianoacetat d'etil es pot preparar per l'acció del cianur de sodi o de potassi sobre el cloroacetat d'etil i per l'acció del cianur de sodi sobre el cloroacetat de sodi, seguida d'esterificació. |
| Descripció general |
Un líquid incolor. Més dens que l'aigua. El contacte pot irritar la pell, els ulls i les mucoses. Punt d'inflamació 210 graus F. Pot ser tòxic per ingestió. S'utilitza per fer altres productes químics. |
| Reaccions de l'aire i l'aigua |
Lleugerament soluble en aigua. |
| Perfil de reactivitat |
El cianoacetat d'etil és alhora un nitril i un èster. Els èsters reaccionen amb els àcids per alliberar calor juntament amb alcohols i àcids. Els àcids oxidants forts poden provocar una reacció vigorosa que sigui prou exotèrmica per encendre els productes de la reacció. També es genera calor per la interacció d'èsters amb solucions càustiques. L'hidrogen inflamable es genera barrejant èsters amb metalls alcalins i hidrurs. Els nitrils poden polimeritzar en presència de metalls i alguns compostos metàl·lics. Són incompatibles amb els àcids; barrejar nitrils amb àcids oxidants forts pot provocar reaccions extremadament violentes. Els nitrils són generalment incompatibles amb altres agents oxidants com ara peròxids i epòxids. La combinació de bases i nitrils pot produir cianur d'hidrogen. Els nitrils s'hidrolitzen tant en àcid com en base aquós per donar àcids carboxílics (o sals d'àcids carboxílics). Aquestes reaccions generen calor. Els peròxids converteixen els nitrils en amides. Els nitrils poden reaccionar vigorosament amb agents reductors. L'acetonitril i el propionitril són solubles en aigua, però els nitrils superiors al propionitril tenen poca solubilitat aquosa. També són insolubles en àcids aquosos. |
| Perill |
Tòxic per ingestió i inhalació. |
| Perill per la salut |
TÒXICS; La inhalació, la ingestió o el contacte (pell, ulls) amb vapors, pols o substàncies poden causar lesions greus, cremades o la mort. El contacte amb la substància fosa pot causar cremades greus a la pell i als ulls. La reacció amb aigua o aire humit alliberarà gasos tòxics, corrosius o inflamables. La reacció amb l'aigua pot generar molta calor que augmentarà la concentració de fums a l'aire. El foc produirà gasos irritants, corrosius i/o tòxics. L'escorriment de l'aigua de control d'incendis o de dilució pot ser corrosiu i/o tòxic i provocar contaminació. |
| Perill d'incendi |
Material combustible: pot cremar però no s'encén fàcilment. La substància reaccionarà amb l'aigua (algunes de manera violenta) alliberant gasos inflamables, tòxics o corrosius i escorrentia. Quan s'escalfen, els vapors poden formar mescles explosives amb l'aire: perill d'explosió a l'interior, a l'exterior i a les clavegueres. La majoria dels vapors són més pesats que l'aire. S'escamparan per terra i es recolliran en zones baixes o reduïdes (clavagueres, soterranis, dipòsits). Els vapors poden viatjar a la font d'ignició i retrocedir. El contacte amb metalls pot produir un gas hidrogen inflamable. Els contenidors poden explotar quan s'escalfen o si estan contaminats amb aigua. |
| Perfil de seguretat |
oís per ingestió. Moderadament tòxic per via intraperitoneal i subcutània. Combustible quan s'exposa a la calor o la flama; pot reaccionar amb materials oxidants. Wdl reacciona amb l'aigua o el vapor per produir vapors tòxics i inflamables. Per combatre el foc, utilitzeu CO2, químic sec. Quan s'escalfa fins a la descomposició o en contacte amb fums àcids o àcids, emet fums altament tòxics de CN-. Vegeu també NITRILS. |
| Exposició potencial |
Nitril utilitzat per fabricar colorants, productes farmacèutics i altres productes químics. |
| Primers auxilis |
Si aquesta substància química entra als ulls, traieu les lents de contacte alhora i irrigueu immediatament durant almenys 15 minuts, aixecant de tant en tant les parpelles superiors i inferiors. Busqueu atenció mèdica immediatament. Si aquest producte químic entra en contacte amb la pell, traieu-vos la roba contaminada i renteu-vos immediatament amb aigua i sabó. Busqueu atenció mèdica immediatament. Si s'ha inhalat aquest producte químic, retireu-lo de l'exposició, comenceu a respirar de rescat (utilitzant precaucions universals, inclosa la màscara de reanimació) si la respiració s'ha aturat i la RCP si l'acció del cor s'ha aturat. Trasllat immediatament a un centre mèdic. Quan s'ha empasat aquesta substància química, busqueu atenció mèdica. Donar grans quantitats d'aigua i provocar el vòmit. No feu vomitar una persona inconscient |
| emmagatzematge |
re ubicació del verí. Abans de treballar amb aquest producte químic, hauríeu d'estar entrenat sobre la seva correcta manipulació i emmagatzematge. Emmagatzemar en recipients ben tancats en una àrea fresca i ben ventilada, lluny d'oxidants, bases fortes, àcids forts, agents reductors, humitat i fonts d'ignició. Quan sigui possible, bombeu automàticament el líquid dels bidons o altres contenidors d'emmagatzematge per processar els contenidors. |
| Enviament |
UN3276 Nitrils, líquids, tòxics, nos, Classe de perill: 6.1; Etiquetes: 6.1-Matèries tòxiques, Nom tècnic obligatori, Perill potencial d'inhalació (disposició especial 5). |
| Mètodes de purificació |
Agitar l'èster diverses vegades amb Na2CO3 aquós al 10%, rentar-lo bé amb aigua, assecar-lo amb Na2SO4 i destil·lar-lo fraccionament. [Beilstein 2 IV 1889.] |
| Incompatibilitats |
Incompatible amb oxidants (clorats, nitrats, peròxids, permanganats, perclorats, clor, brom, fluor, etc.); el contacte pot provocar incendis o explosions. Mantenir allunyat de materials alcalins, bases fortes, àcids forts, oxoàcids, epòxids i agents reductors. Els nitrils poden polimeritzar en presència de metalls i alguns compostos metàl·lics. Són incompatibles amb els àcids; barrejar nitrils amb àcids oxidants forts pot provocar reaccions extremadament violentes. Els nitrils són generalment incompatibles amb altres agents oxidants com ara peròxids i epòxids. La combinació de bases i nitrils pot produir cianur d'hidrogen. Els nitrils s'hidrolitzen tant en àcid com en base aquós per donar àcids carboxílics (o sals d'àcids carboxílics). Aquestes reaccions generen calor. Els peròxids converteixen els nitrils en amides. Els nitrils poden reaccionar vigorosament amb agents reductors. L'acetonitril i el propionitril són solubles en aigua, però els nitrils superiors al propionitril tenen poca solubilitat aquosa. També són insolubles en àcids aquosos. Reacciona amb la humitat, l'aigua i el vapor, formant fums tòxics. |
| Eliminació de residus |
Consulteu amb les agències reguladores ambientals per obtenir orientació sobre pràctiques d'eliminació acceptables. Els generadors de residus que contenen aquest contaminant (més o igual a 100 kg/mes) han de complir amb les regulacions de l'EPA que regulen l'emmagatzematge, el transport, el tractament i l'eliminació de residus. |