| Descripció |
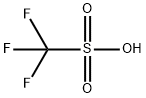
L'àcid trifluorometanosulfònic, també conegut com àcid triflic, TFMS, TFSA, HOTf o TfOH, és un àcid sulfònic amb la fórmula química CF3SO3H. Sovint es considera un dels àcids més forts, i és un dels anomenats "superàcids". s'utilitza en la fabricació de productes farmacèutics, productes químics agrícoles i polímers. La forma anhidra s'utilitza àmpliament en la síntesi química fina. No és oxidant, té una alta estabilitat tèrmica i és resistència tant a l'oxidació com a la reducció, la qual cosa el converteix en un dels compostos més útils de la classe dels súper àcids. A la indústria farmacèutica, s'utilitza per fer una sèrie de classes de fàrmacs, inclosos nucleòsids, antibiòtics, esteroides, proteïnes i glicòsids. L'anhídrid triflic reacciona fàcilment amb l'aigua i té un perfil de toxicitat desfavorable. |
| Propietats químiques |
L'àcid trifluorometanosulfònic és un líquid higroscòpic i incolor a temperatura ambient. És soluble en dissolvents polars com la dimetilformamida (DMF), el dimetilsulfòxid (DMSO), l'acetonitril i la dimetilsulfona. L'addició d'àcid tríflic als dissolvents polars pot ser perillosament exotèrmica.
L'àcid trifluorometanosulfònic s'utilitza àmpliament, especialment com a catalitzador i precursor en química orgànica. Amb un Ka=8. 0 1014 (pKa ~ -15) mol/kg, HOTf es qualifica com a superàcid. L'àcid triflic deu moltes de les seves propietats útils a la seva gran estabilitat tèrmica i química. Tant l'àcid com la seva base conjugada CF3SO3-, coneguda com a triflat, resisteixen les reaccions d'oxidació/reducció, mentre que molts àcids forts s'estan oxidant, per exemple, HClO4 i HNO3. L'anió triflat és immune a l'atac fins i tot de nucleòfils forts. A causa de la seva resistència a l'oxidació i reducció, l'àcid tríflic és un reactiu molt útil i versàtil. A més, recomanant el seu ús, l'àcid triflic no sulfona els substrats, cosa que pot ser un problema amb l'àcid sulfúric, l'àcid fluorosulfúric i l'àcid clorosulfònic. A continuació es mostra una sulfonació prototípica, que HOTf no pateix: C6H6 + H2SO4 → C6H5(SO3H) + H2O. |
| Preparació |
Líquid groc-marró. El punt d'ebullició és de 167 ~ 170 graus. L'índex de refracció és 1,331. La densitat relativa és 1,708. És els àcids orgànics més forts, fàcilment solubles en aigua. Utilitzeu disulfur de carboni com a matèria primera, amb la reacció del pentafluorur de iode per produir disulfur de trifluorometil. .(CF3S) Es va obtenir 2Hg en reaccionar amb el mercuri; Després, mitjançant l'oxidació de l'òxid d'hidrogen, s'adquireix àcid trifluorometanosulfònic. |
| Usos |
S'utilitza per a la síntesi orgànica, àmpliament utilitzat en la indústria farmacèutica i química, com ara nucleòsids, antibiòtics, esteroides, proteïnes, sucre, síntesi de vitamines, modificació del cautxú de silicona.
Isomerització i alquilació del catalitzador, la preparació de 2, 3-dihidro-2-indanona, tetralona, glicòsids en l'eliminació de glicoproteïnes.
|
| Reaccions |
L'àcid trifluorometanosulfònic actua com a catalitzador per a les reaccions d'esterificació i un valorant àcid en la valoració àcid-base no aquosa. És útil en protonacions a causa de la presència de base conjugada triflat no és nucleòfil. Serveix com a agent desglicosilant de les glicoproteïnes. A més, és un precursor i un catalitzador de la química orgànica. Reacciona amb halogenurs d'acil per preparar anhídrids triflats mixts, que són agents acilants forts utilitzats en les reaccions de Friedel-Crafts. Actua com a material de partida clau per a la preparació d'èters i olefines per reacció amb alcohols, així com per preparar anhídrid trifluorometanosulfònic per reacció de deshidratació.
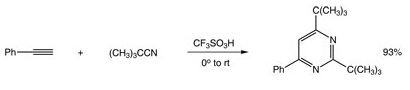
Catalitzador utilitzat en la producció de substitut de mantega de cacau a partir d'oli de palma. Aquesta és una reacció molt similar a la que es faria si es volgués crear polímers utilitzant àcid tríflic en la síntesi. Altres reaccions de tipus Friedel-Crafts que utilitzen àcid tríflic inclouen el craqueig d'alcans i l'alquilació d'alquens, que són molt importants per a la indústria del petroli. Aquests catalitzadors derivats d'àcid tríflic són molt efectius per isomeritzar hidrocarburs de cadena recta o lleugerament ramificats que poden augmentar l'octani d'un determinat combustible basat en petroli. |
| Propietats químiques |
Líquid clar de color groc molt clar. Fum a l'aire, fàcil d'absorbir aigua per formar un hidrat. És fàcilment soluble en aigua, allibera molta calor i s'hidrolitza per generar trifluorometà (CHF3) i àcid sulfúric. |
| Usos |
Com a catalitzador en reaccions d'acilació, alquilació i polimerització tipus Friedel-Crafts; com a dissolvent per a l'ESR; com a valorant àcid fort no aquós; amb àcid trifluoroacètic, qv, en síntesi de pèptids en fase sòlida. Un dels àcids monopròtics més forts disponibles. |
| Usos |
L'àcid trifluorometanosulfònic actua com a catalitzador per a les reaccions d'esterificació i un valorant àcid en la valoració àcid-base no aquosa. És útil en protonacions a causa de la presència de base conjugada triflat no és nucleòfil. Serveix com a agent desglicosilant de les glicoproteïnes. A més, és un precursor i un catalitzador de la química orgànica. Reacciona amb halogenurs d'acil per preparar anhídrids triflats mixts, que són agents acilants forts utilitzats en les reaccions de Friedel-Crafts. Actua com a material de partida clau per a la preparació d'èters i olefines per reacció amb alcohols, així com per preparar anhídrid trifluorometanosulfònic per reacció de deshidratació. |
| Definició |
ChEBI: l'àcid trifluorometanosulfònic és un compost d'un carboni que és l'àcid metanosulfònic en el qual els hidrògens units al carboni metil han estat substituïts per fluors. És un compost d'un carboni i un àcid perfluoroalcansulfònic. És un àcid conjugat d'un triflat. |
| Descripció general |
L'àcid trifluorometanosulfònic és un àcid orgànic fort. Es pot preparar fent reaccionar bis(trifluorometiltio)mercuri amb H2O2. En barrejar amb HNO3, proporciona un reactiu nitratant (una sal de nitroni). Aquest reactiu és útil per a la nitració de compostos aromàtics. S'ha estudiat la seva dissociació en diversos dissolvents orgànics. |
| Perfil de seguretat |
Un irritant corrosiu per a la pell, els ulls i les mucoses. Un àcid fort. La reacció violenta amb clorurs d'acil o hidrocarburs aromàtics genera clorur d'hidrogen gasós tòxic. Quan s'escalfa fins a la descomposició, emet fums tòxics de Fand SOx. Vegeu també FLUORURS. |