| Descripció |
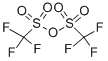
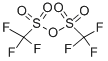
L'anhídrid trifluorometanosulfònic, també conegut com a anhídrid triflic, ha demostrat ser un reactiu extraordinari per a una àmplia gamma de transformacions. Com a reactiu comercial i fàcilment disponible, s'ha utilitzat àmpliament en química sintètica a causa de la seva alta electrofilia. Donada la seva alta afinitat cap als O-nucleòfils, s'afavoreix molt la reacció amb alcohols, carbonils, òxids de sofre, fòsfor i iode cap a la formació dels triflats corresponents. Com un dels principals grups de sortida de la química orgànica, els triflats generats obren la porta a diverses transformacions aigües avall, incloses (però no limitades a) reaccions de substitució, processos d'acoblament creuat, reaccions redox i reordenaments[1-2] . |
| Propietats químiques |
líquid clar incolor a marró clar |
| Usos |
L'anhídrid trifluorometanosulfònic és un electròfil fort utilitzat en la síntesi química per introduir el grup triflil. |
| Usos |
L'anhídrid trifluorometanosulfònic s'utilitza per convertir fenols i imina en èster triflic i grup NTf. És un electròfil fort utilitzat per a la introducció del grup triflil en la síntesi química. Serveix com a reactiu en la preparació de triflats d'alquil i vinil, i per a la síntesi estereoselectiva de donants d'uronat de metil manosazida. Actua com a catalitzador de la glicosilació amb hidroxisucres anomèrics per preparar polisacàrids. |
| Definició |
ChEBI: l'anhídrid tríflic és un anhídrid organosulfònic. Està relacionat funcionalment amb un àcid triflic. |
| Perfil de reactivitat |
L'activació electròfila d'amides terciàries i secundàries amb anhídrid tríflic (Tf2O; anhídrid rifluorometanosulfònic) en condicions suaus dóna lloc a triflats d'imini i imino, respectivament, que es podrien utilitzar com a reactius versàtils per reaccionar amb diversos C-, N-, O- i S. -nucleòfils per a la transformació d'una funció amida en diferents productes. Altres nucleòfils que contenen oxigen, com els sulfòxids i els òxids de fòsfor, també podrien patir un atac nucleòfil amb Tf2O per generar triflat de tioni, espècies P electròfiles i triflat de fosfoni. Aquestes espècies transitòries altament actives podrien experimentar fàcilment reaccions de substitució nucleòfila per a més transformacions diverses. A més, a causa de la forta propietat electròfila, el Tf2O és propens a reaccionar amb nucleòfils relativament febles, com ara grups nitril o alguns compostos heterocíclics que contenen nitrogen. A més, el Tf2O també s'ha utilitzat com a reactiu de trifluorometilació radical i trifluorometiltiolació mitjançant l'alliberament de SO2 o procés de desoxigenació per a la síntesi de compostos trifluorometilats i trifluorometiltiolats[2]. |
| Perill |
Pot ser corrosiu per als metalls. Nociu per ingestió. Provoca cremades greus a la pell i danys als ulls. |
| Inflamabilitat i Explosibilitat |
No classificat |
| Síntesi |
La síntesi de l'anhídrid trifluorometanosulfònic és la següent:
Un matràs sec de fons rodó de {{0}}ml. es carrega amb 36,3 g. (0,242 mol) d'àcid trifluorometanosulfònic (Nota 1) i 27,3 g. (0,192 mol) de pentòxid de fòsfor (Nota 2). Es tanca el matràs i es deixa reposar a temperatura ambient durant almenys 3 hores. Durant aquest període la mescla de reacció canvia d'una massa a una massa sòlida. El matràs està equipat amb un capçal de destil·lació de recorregut curt i s'escalfa primer amb un corrent d'aire calent d'una pistola de calor i després amb la flama d'un petit cremador.El matràs s'escalfa fins que no es destil·li l'anhídrid trifluorometanosulfònic, pb 82–115 graus, donant 28,4–31,2 g. (83-91%) de l'anhídrid, un líquid incolor. Tot i que aquest producte és prou pur per utilitzar-lo en el següent pas, l'àcid restant es pot eliminar de l'anhídrid mitjançant el procediment següent. Un purí de 3,2 g. de pentòxid de fòsfor en 31,2 g. de l'anhídrid brut s'agita a temperatura ambient en un matràs amb tap durant 18 hores. Després d'haver equipat el matràs de reacció amb un capçal de destil·lació de recorregut curt, s'escalfa amb un bany d'oli, donant 0,7 g. de precurs, pb 74–81 graus, seguit de 27,9 g. de l'anhídrid de l'àcid trifluorometanosulfònic pur, pb 81-84 graus.

|
| emmagatzematge |
Emmagatzemar en un lloc fresc, sec i ben ventilat. Sensible a la humitat. |
| Mètodes de purificació |
Es pot preparar recentment a partir de l'àcid anhidre (11,5 g) i P2O5 (11,5 g, o la meitat d'aquest pes) deixant-lo de banda a temperatura ambient durant 1 hora, destil·lant els productes volàtils i després destil·lant-lo a través d'una curta columna Vigreux. És fàcilment hidrolitzat per H2O i es descompon apreciablement al cap d'uns dies per alliberar SO2 i produir un líquid viscós. Emmagatzemeu-lo sec a baixes temperatures. [Burdon et al. J Chem Soc 2574 1957, Beard et al. J Org Chem 38 373 1973, Beilstein 3 IV 35.] |
| Referències |
[1] Haoqi Zhang. "Anhídrid trifluorometanosulfònic en l'activació d'amida: una eina poderosa per forjar nuclis heterocíclics". TCIMAIL (2021).
[2] Dr. Qixue Qin, Prof. Dr. Ning Jiao, Zengrui Cheng. "Aplicacions recents de l'anhídrid trifluorometanosulfònic en la síntesi orgànica". Angewandte Chemie 135 10 (2022). |